ANDA制剂研发中QbD与DOE的运用(葛季声、杨东、汤丽娟与褚襄萍等博士干货分享)
导读:
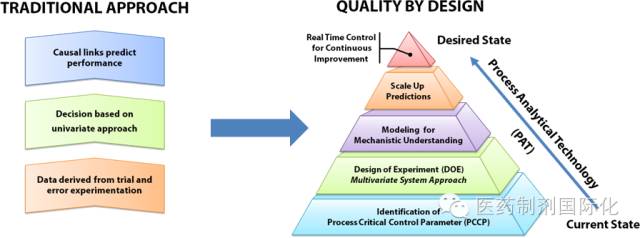
质量源于设计 (QbD) 理念随着ICH和FDA的推广在制剂研发中逐渐被采用。FDA对ANDA申请需要体现QbD理念的要求从2009年发布指导原则到2013年1月起正式执行。QbD理念将贯穿整个产品研发过程,要对原料、处方、工艺各因素属性做影响评估,使用包括DOE等手段建立合理的设计空间,在产品的整个生命周期中应用恰当的控制策略。
2016年9月24日20:30-22:30,ANDA制剂研发专家葛季声博士、杨东博士、汤丽娟博士,还有褚襄萍博士给各位药友分享了他们在 [ANDA制剂研发中QbD与DOE的运用] 的宝贵经验。
[主要人员介绍]
葛季声博士:美国V&M Pharmtech威和麦公司合伙人。曾担任亚宝药业北京研究院制剂研发总监及研究院副院长,负责亚宝药业仿制药国际化项目。葛博士对FDA有关ANDA仿制药的政策法规演变非常了解,对QbD理念在ANDA研发中的运用熟悉且颇有见地。
杨 东博士:华海美国Prinston Pharma制剂研发总监。扬子江药物研究院原副院长,杨东博士长期活跃在学术界和产业界,对ANDA制剂开发中QBD理念及DOE设计的运用非常精通。
汤丽娟博士:美国法明乐实验室总裁兼首席科学家。浙江京新药业制剂国际化业务合作伙伴。汤博士在高端仿制药和缓控释制剂以及难溶药物产品研发方面经验丰富,对ANDA开发过程中QbD的运用十分熟悉。值得一提的是,汤博士在文学和艺术方面也有很高的造诣。
褚襄萍博士:上海海翔制剂研发总监,在讨论中担任话题主持。褚博士现参与海翔药业的制剂国际化业务,在QbD和DOE方面有很多实际运用经验和心得。
陈家松先生: SAS公司高级顾问。DOE的科学合理应用需要制剂科学知识与经验,和数学统计知识的有机结合。陈顾问将从数据统计分析的角度给大家回答相关问题。陈老师也致力于推广JMP软件的运用。
小望-望开鹏:制剂国际化ANDA研发新兵,主修口服缓控释制剂与经皮给药制剂。业余着力于医药制剂国际化跟踪与传播。“制剂国际化”系列讨论参与人。(微信加281660433验证参与更多交流)
其他参与嘉宾:
徐 坚老师:上海臣邦医药研发总监。原恒瑞医药制剂国际化业务药政负责人,有丰富的制剂国际化经验。
李洪明博士: 浙江海翔药业副总经理,研究院院长。
[讨论前提纲]
“迎接ANDA制剂研发的变革,解码QBD与DOE之迷思”研讨会邀您和3位大咖一起探讨:
1. QBD的关键要点是风险评估,是靠主观的经验判断评估,还是借助量化评分工具。如何厘清关键影响因素与变量,设计出合理的QBD方案。
2. 小试规模做DOE不靠谱,中试规模做DOE不合算,设计何时做最有效最科学。
3. 设计要做多少,做到什么程度。对于工艺步骤较多的复杂产品,每一个步骤都包含处方的考量,工艺的考量,还有不同步骤前后结合的影响。如FDA发布的缓释制剂QBD案例中,上药工序的工艺研究,在4kg的小试规模,选取4个因素,以部分因子设计做了11次实验。在上药阶段的40kg规模中试放大中,又以3个显著因素,以部分因子设计进行了5次实验。缓释微丸包衣工序也重复了同样的做法。如何应对如此庞大的试验量。
4. 全因子析因设计,部分因子析因设计,响应面设计,田口设计,混料设计,Plackett-Burman试验,单因素试验,还有其他设计等等,如何结合具体情况巧妙选择,减少试验次数,得到较优结果。
5. 如何辩证看待DOE实验和BE结果的关系。是产品开发前期就通过有效的设计来优化处方工艺,提高BE成功率。还是使用通过BE之后确定的处方工艺来做设计空间的研究。
由于时间紧凑,并结合现场提问角度,部分问题不易展开,后续可继续交流。以下是讨论内容的精简编辑。
1[FDA对QbD理念实施的要求]
望开鹏:
首先,我问一个小的问题,FDA对ANDA申请需要体现QbD理念的要求从2013年1月起执行,这是否代表以后所有产品需要体现QbD的设计理念,或者说QbD是必须具备的了。
葛季声:
是的。过去是QbT,现在是QbD。 QbT:Quality by Test。
小望-望开鹏:
“质量来自检测”转换到“质量源于设计”了。
葛季声:
这个转换对做制剂的影响很大,过去知道配方、工艺,做一批中试通过检验,过BE就可申报,做制剂的有配方很牛。现在FDA啥都要问个Why,十万个为什么。
杨东-华海美国:
目前的申报部门的信息,基本上是不采用QbD概念进行的研发,FDA拒绝的机会很大。
小望-望开鹏:
现在要求是,QbD理念将贯穿整个产品研发过程,对原料、处方、工艺各因素属性做影响评估,使用包括DOE等手段建立合理的设计空间,在产品的整个生命周期中应用恰当的控制策略。
杨东-华海美国:
这是FDA申报的要求。对于国内全面实行QbD概念,估计还需要一些时间。
汤丽娟-Pharmula Lab:
其实好的制剂研发一直就应当有系统的研究,QbD成为FDA推广的一种模式,但这并沒有否定其它研究模式,所以我不认为存在绝对的衔接问题。实验做得到位,能够解决问题,数据处理科学,FDA不会不接受。关键是设计实验的人,知道自己在做什么,和为什么做。
2[DOE实验设计方法的选择]
李峰-广州新济:
各位老师好,想请教DOE过程中如何选择用何种实验设计方法?
陈家松-SAS:
传统实验设计的方法按照其实验的主要目的大致可以分为两大类:
第一类:关键因子筛选优化设计(目前没有统一的名称)
1. 筛选因子:从大量的潜在因子中找到关键因子,重点考量因子的主效应,交互作用。如:
a. 全因子析因设计
b. 部分因子析因设计
c. Plackett-Burman设计
d. 单因素设计
2. 优化:针对关键因子进一步分析,探索优化方案,如:
a. 响应曲面设计
b. 空间填充设计
以及第二类:非线性设计。
3[QbD和DOE在小试阶段与中试阶段的运用]
王峰-制剂学人:
QbD在小试阶段还好弄,车间技转后怎么做啊…
杨东-华海美国:
我们现在要求DOE要在lab scale完成。对于DOE,我们一般会在lab scale阶段完成。Lab scale, 规模是生产规模的1/100。
汤丽娟-Pharmula Lab:
@杨东 Prinston Pharm 同意,小试阶段的数据对提供QbD的支持也很重要。
张玉-默克:
小试DOE主要能筛选关键影响及找到影响大小,具体中试参数还是要scale up。
褚襄萍-海翔:
我的经验是:Lab Scale 处方筛选DOE可行有效,工艺优化DOE在生产设备上。
杨东-华海美国:
中试规模的DOE成本高,对于brand name product, 我们的确这样做,甚至在manufacture scale做DOE。如果大家看到新药(brand name)的试验方案,大家肯定是被惊呆了。但是,仿制药为了降低成本,我们需要将DOE在Lab scale 完成。
褚襄萍-海翔:
杨博,中试成本确实高,我目前也只在压片工艺做了DOE,因为相对其他工艺成本低。而且因为我们的压片机非常稳定,时间也是比FDA模板缩短了的。
杨东-华海美国:
中试阶段是对于lab scale得到的控制方案的认证阶段。
反向工程(Reverse Engineering)阶段:
目标产品质量指标(QTPP)的建立
Establishment of QualityTarget Product Profile
小试(Lab Scale Batch)阶段:
关键质量控制参数的筛选和确认
Screening and Identification of CQA Controlling Factors
关键质量控制参数控制方案的建立
Establishment of CQA Controlling Strategy
中试技术批(Technical Batch):
中试规模的CQA的控制方案的确认和QTPP的确认
Establishment of Quality Target Product Profile
杨东-华海美国:
大家认为小试DOE不靠谱的依据是什么?
王峰-制剂学人:
CQA分析得不到位?
丁纪钱-连云港:
小试主要担心噪音,因为小试设备,环境温湿度,检测方法等等。
葛季声:
好多DOE实验失败都是因为“噪音”问题。
实验成功的要素:
-信号还是噪音?
-复杂系统工程实验数据的误差。
SQRT(数据)
= ∑SQRT (各种因素)i
i= 人工、环境、机器、仪器、方法、工艺、材料物化性质等.
如何减少噪音?
- 人员培训
- 控制环境(湿度、温度)
- 仪器校正
- 分析方法验证
汤丽娟-Pharmula Lab:
@葛季声 同意。噪音问题很重要。
褚襄萍-海翔:
关于噪音:日本的田口玄一(Genichi Taguchi)博士在参数设计方法方面贡献非常突出,他在设计中引进 SN比(信噪比)的概念,并以此作为评价参数组合优劣的一种测度,这是很有价值的,以至于很多文献和软件都把稳健参数设计方法称为田口设计(Taguchi Design)。
陈家松-SAS:
如果“噪音”成为影响DOE效果的因素的话,有必要前期识别,加以控制。
丁纪钱-连云港:
噪音过大可能影响结果的判断和分析,所以对于小试如何设计DOE比较迷惑。
汤丽娟-Pharmula Lab:
@丁纪钱: QbD不是一次实验,而是从头到尾不断地实验。
葛季声:
另外,选择正确的“信号”也很关键。
“信号” = 实验结果
”信号”的定量表征:
- 溶出曲线(度)
- 颗粒度,颗粒分布
- 包衣厚度
- 片重,磨损度,硬度,分片
- 物化稳定性、杂质含量
- ……
小望-望开鹏:
很多处方到了中试都要做一定调整。
褚襄萍-海翔:
小望,的确是这样,有些处方剂型的溶出受工艺影响较大,中试之后处方有可能调整,但是不影响我们在小试特定工艺条件下的DOE结论,可以在这个基础上继续优化处方,科学理解是循序渐进的。
葛季声:
对,这就是QbD的核心。
杨东-华海美国:
是的,中试是对于控制方案的优化和验证。
陈家松-SAS:
的确制剂优化方案的效果需要工艺条件的验证才更有说服力。
杨东-华海美国:
产品的质量和process的可行性主要决定于处方。在早期需要解决处方-工艺匹配度问题。
汤丽娟-Pharmula Lab:
@杨东 Prinston Pharm 产品的质量和process的可行性主要决定于处方。非常同意你的观点。
杨东-华海美国:
所以,就是处方的选择阶段,我们也会同时进行工艺区间的评价。
汤丽娟-Pharmula Lab:
这个认识对于国内同行非常重要。
杨东-华海美国:
也就是不出实验室,大家应该知道我的处方在设备上运行的性质。工艺处方不分离,是原则。
褚襄萍-海翔:
处方优化阶段也要解决process feasibility。
汤丽娟-Pharmula Lab:
我接触的国内研发流程不符合这个设计。我认为这是国内放大失败率高的原因。
葛季声:
做小试是就想着上中试、生产线的工艺可行性,是有经验的制剂人应有的思维。
汤丽娟-Pharmula Lab:
国内的老板认为,我拿到一个处方,或者是原研的处方就一定可以在我的厂生产出来。其实,设备不同,不仅仅是工艺参数的问题,处方更是主要问题。
葛季声:
还是老思维,比QbT还老。
小望-望开鹏:
还有一个情况,有的人的做法是通过了BE再做DOE来证明当初的设计是较优的。很多人的希望是先找出目标处方,对上溶出,通过BE。然后做很多需要补充的实验或者优化。
毕立军-深圳致君:
从处方工艺看不出BE结果,万一BE不行,处方优化不就白做了吗。
杨东-华海美国:
我们可以用溶出作为BE的判断。
葛季声:
如果不知道“噪音”变量,做出BE批以后也会出问题,亲历好多案例,反而减缓上市争时间。
杨东-华海美国:
同意 @葛季声。
汤丽娟-Pharmula Lab:
没有经过生产型设备运行,没有确定配方在生产设备上有可接受的参数区间就没有配方。所以制剂的研发不是小试,中试,生产的三段式。而是研发,证实,和申报批确认这个三段式的。
杨东-华海美国:
不知道大家是否熟悉Scale Down?
Scale Down就是根据生产该产品的生产线的条件和工艺区间,采用Scale Down逆向的方法,预测小试的实验条件。是确保小试的工艺条件在放大后能够在现有生产条件下生产。
丁纪钱-连云港:
@杨东 Prinston Pharm 这种逆推非常值得学习,往往小试都不看中试设备,一切只看溶出结果。
汤丽娟-Pharmula Lab:
小试只看溶出是没用的。上设备以后要改处方怎么办?
葛季声:
希望做制剂的多去工厂参与中试,很受益。我在国内同别人讲国外博士都在第一线做中试,还有好多人当笑话。
丁纪钱-连云港:
国内的某些博士都是坐办公室,国外比如各位老师,丁某还奋斗在一线。
褚襄萍-海翔:
杨博,小试和中试设备原理相同的情况下scale down,那么小试设备做工艺优化DOE就可行了,您们目前是这个策略?
杨东-华海美国:
是的 @褚博。
丁纪钱-连云港:
而且中试设备都会进行变更,有些设备可能因为车间原因,和小试设备原理不尽一致,参数包括处方都可能变化,所以对DOE的设计很迷惑。如果小试设备和某些不可抗因素导致无法和大生产设备相匹配该怎么办?
丁纪钱-连云港:
国内这种情况比较多。尤其是像湿法制粒,流花床的设备,老车间和新建车间都无法和小试设备都很难在参数调节甚至原理上一致,尤其是当我们小试用进口设备,中试用国产设备时。
褚襄萍-海翔:
是的,比如流化床,小试和中试,生产设备必须同样设计,要有这个条件很难。
葛季声:
回答上面问题,一般小试和中试的设备最好是同一厂家、原理相同。但就这样小试到中试还是有些经验、技巧在内。记住一点:机械动力学同设备大小不是线性关系。
褚襄萍-海翔:
非常同意葛博,机械动力学同设备大小不是线性关系。需要经验和理论相结合。
4[QbD和DOE的实施,关键工艺参数与响应量的筛选]
任传杰-山东齐都:
请问:确定处方DOE筛选的小试基础工艺参数有什么好的经验?
杨东-华海美国:
回答刚才对于小试DOE参数的选择方法:通过Risk Assessment。
任传杰-山东齐都:
@杨东 Prinston Pharm Q9的方法是吧?
葛季声:
风险评估方法:
- 基于过去的经验(Prior Knowledge)
- 应用科学知识(Scientific Understanding)
评估工具:
- 半经验判断
- 鱼骨图(Ishikawa Diagram)
- FMEA(Failure
Mode Effects Analysis)
杨东-华海美国:
把所有的处方因素和工艺因素列表,组织大家brain storm。让大家讨论每个因素的影响,确定主要因素、次主要因素、和非主要因素。将主要和次主要列入DOE考察范围。
丁纪钱-连云港:
风险评估、QbD、DOE设计是否允许加入个人经验来呢?
葛季声:
容许加个人经验。
杨东-华海美国:
是的,根据经验。这个时候的经验就很重要了。
丁纪钱-连云港:
因为实际操作时,风险评估好多时候开始需要经验判断,然后后期通过实验结果重新对风险进行修正。
王峰-制剂学人:
请教各位,除了常用的溶出和释放相似因子,还有哪些response variable 值得上DOE优化?
Polymers-程亮:
@王峰-制剂学人 均匀度,有关物质,看开发的技术特性。
葛季声:
要看具体的配方,如果有因素影响稳定性,也可做杂质。
褚襄萍-海翔:
王峰,FDA MR QbD模板上beads coating process,考察的是细粉率和聚集大颗粒率。
5[QbD和DOE的实施,实验量的把握]
小望-望开鹏:
我有一个问题,在我们开发一个仿制药时,做多少量DOE比较合适。对于工艺步骤较多的复杂产品,每一个步骤都包含处方的考量,工艺的考量,还有不同步骤前后结合的影响。
葛季声:
具体做多少,FDA没规定,要根据具体情况定,关键是找到CMA和CPP。
褚襄萍-海翔:
小望,根据风险评估,还有DOE的实际结果。
陈家松-SAS:
具体实验做多少跟要考量的因素的数量,水平都有直接的关系的。
褚襄萍-海翔:
比如:全因子或部分因子DOE模型显著,但是有曲面效应。我们还要继续增加中心点,做曲面响应设计。
陈家松-SAS:
很多专业的实验设计根据都能根据输入的信息结合实验方法进行计算的得出相应的实验次数。
褚襄萍-海翔:
以得到最佳因素水平组合,还要看你的实验目的是什么。实验目的:主效应?交互作用?还是最佳因素水平组合?陈顾问JMP软件有个定制设计可以做到这一点。
陈家松-SAS:
是的,JMP的定制设计可以解决这一类的实验设计要求。它相对于传统的实验设计是一种更为灵活的实验方案构建方法,运用了最优设计的统计理念。
小望-望开鹏:
@杨东 Prinston Pharm 如FDA发布的缓释制剂QBD案例中,上药工序的工艺研究,在4kg的小试规模,选取4个因素,以部分因子设计做了11次实验。在上药阶段的40kg规模中试放大中,又以3个显著因素,以部分因子设计进行了5次实验。缓释微丸包衣工序也重复了同样的做法。如何面对如此大的实验量。
葛季声:
DOE设计不要一下搞太复杂,三因子两级全实验就可。
杨东-华海美国:
Lean QBD: 更加简化和有效的QBD。 It should be lean. 简化的意思。对于仿制药,由于成本控制,lean更为重要。LQBD. low cost QBD = Lean QBD。
Lean QBD就是在运用以前经验的基础上,快速确定和简化试验条件进行的QBD。
6[ANDA申报中QbD与DOE的呈现]
褚襄萍-海翔:
我问一个问题吧:如果因为经验和科学知识足够好,以致于formulation feasibility and process feasibility study就得到了满足要求的处方和工艺,但是因为没有试验设计,不能得到更加科学数据支持的design space来支持control strategy。这种情况下,各位专家,会选择继续DOE完美结论?还是based on scientific evaluation下最终结论?
褚襄萍-海翔:
因为大家知道,我们有SUPAC guidance加上本身对辅料性质功能的理解,有些辅料的比例变化范围是完全可以预测的。
葛季声:
下面谈的话:DOE更多是用来用数据验证成功经验的,用来发现CQA、CPP是要失败的。
褚襄萍-海翔:
如果DOE更多是用来用数据验证成功经验的,所以一个展示的DOE之前可能已经有大量的trial and test。已经基本找到了较优也许不是最优的因素组合。
葛季声:
Trial and test和经验。有时间补个DOE更有说服力。
小望-望开鹏:
使用单因素试验,会不会太难看。
葛季声:
只是显得不“高、大、上”,能做DOE还是要做。
陈家松:
单因素实验有其先天的缺陷,它无法考量不同因素间的交互影响。
褚襄萍-海翔:
陈顾问说得很好,处方不同辅料和工艺的参数之间往往都有交互作用,单因素实验无法准确下结论。全因子和部分因子设计可以帮助我们评估主效应和交互作用。
汤丽娟-Pharmula Lab:
我个人认为,考虑到误差因素,以及因素间相关性问题,单因素实验是最有效,最重要的实验手段之一。强调QbD并不应该否定单因素实验的意义。
代孔恩:
单因素实验在于提取要素,要素都找不到,合理的DOE和QbD以及设计空间都无法落地。
汤丽娟-Pharmula Lab:
@代孔恩 说到了点子上。其实对多个因素逐个考察,放在一起就是一个很好的QbD。
褚襄萍-海翔:
Formulation Feasibility Study阶段单因素实验。
汤丽娟-Pharmula Lab:
我个人的经验,单因素逐个考察是处方筛选的基本,间或插入二个因素部分实验,基本确定处方以后,通过了生产设备的参数要求以后,按照FDA要求QbD或者DOE一下,证明处方的合理性。
7[其他延伸问题—NDA研发中QBD的运用]
丁纪钱-连云港:
对于创新药的QBD同样迷茫,因为国内的创新药一开始可参考资料太少,而且创新药原料药工艺好多时候不稳定,制剂的处方工艺甚至剂型总是变来变去。
王峰-制剂学人:
创新药的QTPP怎么确定比较好,可以应用lean QbD吗?@杨东 Prinston Pharm 国外对创新药的QbD 一般会应用到何种程度?
杨东-华海美国:
好像从2006年的NDA申报需要采用QBD方式,新药的QBD贯穿整个的产品开发过程。
代孔恩:
是的,NDA部分一定需要QBD。
杨东-华海美国:
我们做DOE从小试到中试,我们在生产规模也进行了DOE。
王峰-制剂学人:
@代孔恩 @杨东 Prinston Pharm 那如何确定合适的CQA呢?对于创新药。
杨东-华海美国:
CQA在FDA给的模板中有例子,我们自己也会对于药品的关键属性进行定义。上市产品的设计和开发开始于Phase 2b。主要工作在Phase 3中进行。
代孔恩:
创新药CQA取决于临床方案确定后的暴露形式确定后的制剂形式,确定制剂形式后才能确定CQA。
王峰-制剂学人:
创新药2期3期临床后的规模化生产批次还允许多大的DOE空间?需要补做很多Bridging PK么?
葛季声:
关于生产规模DOE、Design Space, 请看FDA指导。
[结束语]
褚襄萍-海翔:
各位药友和专家,今天三位制剂专家和陈顾问都给了我们很好的DOE在QbD应用经验分享或者见解,对于我们今后的合理QbD制剂工作具有指导和启发意义。也感谢各位药友的积极参与。由于时间关系,今天的集中讨论告一段落。期待我们继续持续共享DOE在QbD制剂开发的经验或者观点。感谢专家的回答和药友的参与。感谢徐老师关注!
葛季声:
谢谢小望、褚博安排,很高兴同杨博、汤博及各位交流,受益非浅。
李洪明-海翔:
非常感谢各位老师,收获很大!
[重要观点补充]
褚襄萍-海翔:
DOE的科学合理应用需要制剂科学知识与经验,和数学统计知识的有机结合。
汤丽娟-Pharmula Lab:
FDA QbD指导原则给出了一个示例,它的风险分析方法和实验设计原则是很好的模型,可以借鉴的。但是其中也有少数不尽合适的地方,机械地模仿这个模板是不合适的。只用统计学试图解决制剂工艺中的关系是完全不够,而且浪费很大。基于化学原理、机械工程解析、和物理以及物理化学的计算和分析是必要的找到关键因素,厘清各因素关系的最重要和最基本的手段。
汤丽娟-Pharmula Lab:
统计学和传统实验流程不矛盾。FDA指导原则对于帮助我们收集数据,从整体的视野归纳分析所有的实验非常好,非常有意义,我们处在大数据时代。但是统计学不能替代制剂学,不能替代我们对制剂处方和工艺的理解。好处方和好工艺还是要靠坚实的制剂基础知识和敏锐的观察分析能力。没有很强的判断和区分能力,不会对实验观察细节和环境,会产生过多的区间外数据。全面的多学科的知识积累加上敏锐的观察和分析能力,是做出好产品的基本功。
参考文献:葛季声博士提供
[1] Guidance for Industry “Q8, Q9, and Q10 Questions and Answers (R4)” FDA Nov, 2011.
[2] Guidance for Industry “Q8, Q9, and Q10 Questions and Answers-Appendix Q&A from Training Sessions” FDA July 2012.
[3] Questions and Answer on Design Space Verification, FDA and EMA, 2013.
[4] Lawrence X. Yu. Pharmaceutical Quality by Design: Product and Process Development, Understanding, and Control. Pharmaceutical Research, Vol. 25, No. 4, p781-791, April 2008.
相关书籍:小望提供
[1] QbD与药品研发:概念与实例. 王兴旺编著. 2014.
[2] 实验设计(DOE) 运用技术指南. 闵亚伦著. 2011
[3] 实验设计与Design-Expert, SPSS的运用. 徐向宏,何明珠主编. 2010.
[嘉宾详细介绍]
葛季声博士 (Dr. Jisheng Ge)简介:
葛季声博士于1985年获得山西大学分子化学硕士学位,1996年在美国依阿华州立大学获化学博士学位。毕业后进入孟山都公司做博士后科学家。葛季声博士在美国从事仿制药研发近二十年,曾任Kremers Urban Pharmaceutical和UPM
Pharmaceutical公司研发总监,负责复杂剂型固体制剂及口腔喷雾剂产品的仿制药研发。在KV Pharmaceutical公司任科学家/资深科学家和项目带头人,从事半固体和口服制剂的研发。在Qualitest Pharmaceutical (现为Endo Pharmaceutical) 公司任主要科学家,开发婴儿口服液和混悬液及半固体仿制药产品。回国后,曾任亚宝药业北京研究院副院长与制剂研发总监,负责亚宝药业仿制药国际化项目。作为独立合同承包人和项目顾问成立V&M Pharmtech美国威和麦公司,与国内企业正在开展深度合作。
杨东博士(Dr. Douglas Yang) 简介:
杨东博士于1995年获得中国药科大学药物化学硕士学位,2005年在美国依阿华大学获药剂学博士学位。杨东博士长期活跃在学术界和产业界。杨博士曾在中国药科大学担任教师,也担任国际重要药学刊物的审评专家。博士毕业后先后工作于美国惠氏,诺华等知名医药公司,作为制药科学家参与产品开发。回国后任职于圣和药业,负责制剂研发工作。曾任扬子江药物研究院副院长。现加盟华海药业美国公司,担任制剂研发总监,负责华海药业ANDA产品开发。
汤丽娟博士简介:
汤丽娟博士于1984年获中国药科大学药物制剂硕士学位,1998年获美国费城药学院药剂学博士学位。汤博士具有30多年的制剂经验,曾先后工作于美国卡乐康、辉瑞、森林实验室、Actavis的Alpharma等公司。在卡乐康工作期间作为专利发明人参与研发了肠溶包衣配方,在Alpharma工作期间,汤博士是抗滥用控释吗啡产品的的专利发明人之一,成功获得加兰他敏片FDA首仿批准和一项专利。2010年汤博士参与组建GHL公司并担任首席科学家,主导两个抗癌冻干粉针剂和七个儿童口服混悬剂的仿制研发。2014年,汤丽娟博士在美国宾夕法尼亚州成立Pharmula Laboratories法明乐实验室,并于2015年8月与浙江京新药业达成战略合作布局制剂国际化,推进高端控释制剂和高难度仿制药在美国FDA的ANDA申报和中国生物等效性产品的研发。值得一提的是,汤博士在文学和艺术方面也具有很高的造诣。
更多讨论请注明身份微信联系281660433,欢迎制剂国际化研发同仁共同交流。
转载请注明:医药制剂国际化--Hi-Drug药聚旗下网站 » ANDA制剂研发中QbD与DOE的运用(葛季声、杨东、汤丽娟与褚襄萍等博士干货分享)